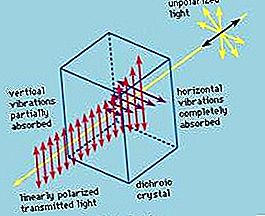
Boranas, bet kuris iš homologinių neorganinių boro ir vandenilio junginių ar jų darinių.
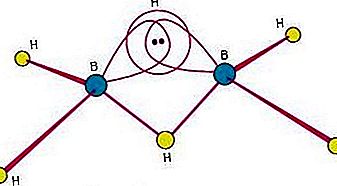
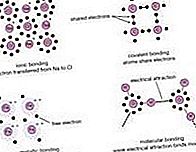
cheminis rišimas: Boranai
Kaip pažymėta anksčiau, elektronų trūkumo junginys diboranas B2H6 gali būti laikomas atomų, laikomų kartu, grupe
Boro hidridai pirmiausia buvo sistemiškai susintetinti ir apibūdinti per 1912 m. Iki maždaug 1937 m. Vokiečių chemiko Alfredo Stocko. Jis juos vadino boranais pagal analogą su alkanais (sočiaisiais angliavandeniliais), anglies hidratais (C), kuris yra boro kaimynas periodinėje lentelėje. Kadangi lengvesnės boranos buvo nepastovios, jautrios orui ir drėgmei bei toksiškos, Stock sukūrė aukšto vakuumo metodus ir aparatus jų tyrimui. Amerikietiškas boranų darbas prasidėjo 1931 m., Kurį atliko Hermannas I. Schlesingeris ir Antonas B. Burgas. Boranai daugiausia domėjosi akademine iki Antrojo pasaulinio karo, kai JAV vyriausybė rėmė mokslinius tyrimus, siekdama rasti lakiųjų urano junginių (borohidridų) izotopų atskyrimui, ir 1950 m., Kai rėmė raketų ir reaktyvinių orlaivių aukštos energijos degalų kūrimo programas. (Boranai ir jų dariniai turi daug didesnį degimo šilumą nei angliavandeniliniai degalai.) William Nunn Lipscomb, jaunesnysis, 1976 m. Gavo Nobelio chemijos premiją už „boranų struktūros tyrimus, išryškinančius cheminio sujungimo problemas“, o vienas iš Schlesingerio. studentai Herbertas Charlesas Brownas pasidalijo 1979 m. prizu už savo hidroboracijos reakciją (1956 m.), nepaprastai lengvu BH pridėjimu3 (atsižvelgiant į BH forma 3 · S) į nesočiųjų organinių junginių (ty alkenus ir alkinus) eteryje tirpiklių (S) kambario temperatūroje, siekiant gauti organoboranes kiekyb (tai yra, reakcijoje gautos visiškai, arba beveik visiškai, iki pabaigos). Hidroboracijos reakcija savo ruožtu atvėrė naujas tyrimų sritis stereospecifinės organinės sintezės srityje.
Stock paruošti boranai turėjo bendrą sudėtį B n H n + 4 ir B n H n + 6, tačiau žinomos sudėtingesnės rūšys, tiek neutralios, tiek neigiamos (anijoninės). Boro hidridų yra daugiau nei bet kurio kito elemento, išskyrus anglį. Paprasčiausias išskiriamas boranas yra B 2 H 6, diboranas (6). (Arabų skaičius skliausteliuose rodo vandenilio atomų skaičių.) Tai yra vienas išsamiausiai ištirtų ir sintetiniu požiūriu naudingiausių cheminių tarpinių junginių. Jis yra parduodamas rinkoje ir daugelį metų tiesiogiai arba netiesiogiai buvo gaminami boranai ir jų dariniai. Laisvieji BH 3 (ir B 3 H 7) yra labai nestabilūs, tačiau juos galima išskirti kaip stabilius adduktus (papildomus produktus) su Lewiso bazėmis (elektronų donoro molekulėmis) - eg, BH 3 · N (CH 3) 3. Boranai gali būti kietos medžiagos, skysčiai arba dujos; paprastai jų lydymosi ir virimo taškai didėja didėjant jų sudėtingumui ir molekulinei masei.
Boranų struktūra ir sujungimas
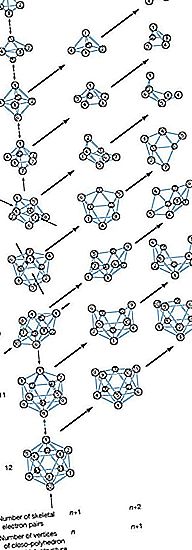
Užuot demonstruodami paprastas anglies junginių grandines ir žiedo konfigūracijas, boro atomai sudėtingesnėse boranose yra išsidėstę daugiakampių kampuose, kurie gali būti laikomi deltaedronais (daugiabriauniai su trikampiais veidais) arba deltaedriniais fragmentais. Ugdytas šių boro grupių suvokimas padėjo chemikams racionalizuoti kitų neorganinių, metalo organinių ir pereinamųjų metalų grupių junginius.
Viena iš kelių nomenklatūros sistemų, kurias pasiūlė Tarptautinė tyrinės ir taikomosios chemijos sąjunga (IUPAC), naudoja būdingus struktūrinius priešdėlius: (1) kloso („clovo“ iš Lotynų Clovis, reiškiančio „narvą“, reiškianti „narvą“, sugadinimas, n boro atomai; (2) nido- (iš lotyniškojo „nidus“, reiškiančio „lizdą“), neuždaromos struktūros, kuriose B n klasteris užima n (1 + 1) kampo daugiakampio kampus, ty uždaro poliardro, kurio viena viršūnė nėra; (3) arachno- (graikų kalba, reiškiančioje „voratinklio tinklą“), dar atviresnės sankaupos, kurių boro atomai užima n (gretimus (n + 2) kampo daugiakampio gretimus kampus, ty uždaro poliardrą su dviem trūkstamais viršūnėmis.; (4) hipofiziniai (graikiškai, reiškiantys „pynimas“ arba „tinklas“), atviriausios sankaupos, kurių boro atomai užima n (3 n) kampu uždaryto uždarojo daugiakampio kampus; ir (5) klado- (graikų kalba, reiškiančiame „atšaka“), n viršūnių, esančių n + 4 viršūnių uždarymo poliaedre, kuriuos užima n boro atomai. Hipofizinių ir klado serijų nariai šiuo metu yra žinomi tik kaip borano dariniai. Ryšį tarp dviejų ar daugiau šių daugiakampių boranų klasterių rodo priešdėlis jungtukas (lotyniškai, reiškiantis „sujungti“). Pavyzdžiui, conjuncto-B 10 H 16 yra gaminamas sujungiant B 3 H 8 vienetų iš dviejų B 6 H 9 molekulės per B-B jungties.
Viena iš didelio susidomėjimo boranų priežastimis yra ta, kad jų struktūros skiriasi nuo bet kurios kitos klasės junginių. Kadangi surišimas boranuose apima daugiacentrį surišimą, kuriame trys ar daugiau atomų turi porą rišančių elektronų, boranai paprastai vadinami medžiagomis, kurių trūkumas yra elektronas. „Diborane“ (6) struktūra yra tokia:
Ši struktūra apima trijų centrų tilto sujungimą, kuriame viena elektronų pora yra dalijama tarp trijų (o ne dviejų) atomų - dviejų boro atomų ir vieno vandenilio atomo. (Žr. Cheminį surišimą: Išplėstiniai cheminio surišimo aspektai: Boranai, skirti aptarti trijų centrų ryšį.) Boro galimybė formuoti tokius ryšius šalia normalių kovalentinių jungčių lemia sudėtingų daugiakampių boranų susidarymą.