Tauriosios dujos, bet kuris iš septynių cheminių elementų, sudarančių periodinės lentelės 18 (VIIIa) grupę. Elementai yra helis (He), neonas (Ne), argonas (Ar), kriptonas (Kr), ksenonas (Xe), radonas (Rn) ir oganessonas (Og). Tauriosios dujos yra bespalvės, bekvapės, beskonės ir nedegios dujos. Jie periodiškai buvo žymimi 0 grupe periodinėje lentelėje, nes dešimtmečius po atradimo buvo manoma, kad jie negali prisijungti prie kitų atomų; tai yra, kad jų atomai negalėjo sujungti su kitų elementų atomais, kad sudarytų cheminius junginius. Jų elektroninės struktūros ir išvados, kad kai kurie iš jų iš tikrųjų sudaro junginius, paskatino paskirti 18 grupę.
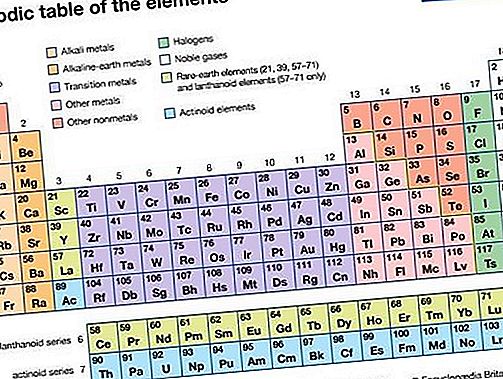
Kai grupės nariai buvo surasti ir identifikuoti, buvo manoma, kad jie yra ypač reti, taip pat chemiškai inertiški, todėl buvo vadinami retomis arba inertinėmis dujomis. Tačiau dabar žinoma, kad keletas šių elementų yra gana gausūs Žemėje ir likusioje visatos dalyje, todėl retas žymėjimas yra klaidinantis. Panašiai termino inertas vartojimas turi trūkumų, kurie reiškia cheminį pasyvumą, o tai rodo, kad 18 grupės junginiai negali būti sudaryti. Chemijoje ir alchemijoje žodis kilnus jau seniai reiškė metalų, tokių kaip auksas ir platina, nenorą chemiškai reaguoti; ta pačia prasme ji taikoma ir čia nurodytai dujų grupei.
Tauriųjų dujų gausumas mažėja didėjant jų atominiam skaičiui. Helis yra pats gausiausias elementas visatoje, išskyrus vandenilį. Visos tauriosios dujos yra Žemės atmosferoje ir, išskyrus helį ir radoną, pagrindinis komercinis jų šaltinis yra oras, iš kurio jos gaunamos skystinant ir frakcinio distiliavimo būdu. Dauguma helio komerciniu būdu gaminami iš tam tikrų gamtinių dujų gręžinių. Radonas paprastai išskiriamas kaip radioaktyviųjų radžio junginių skilimo produktas. Radžio atomų branduoliai spontaniškai suyra, išskirdami energiją ir daleles, helio branduolius (alfa daleles) ir radono atomus. Kai kurios tauriųjų dujų savybės išvardytos lentelėje.
Kai kurios tauriųjų dujų savybės
| helio | neonas | argonas | kriptonas | ksenonas | radonas | ununoctium | |
|---|---|---|---|---|---|---|---|
| * 25.05 atmosferoje. | |||||||
| ** hcp = šešiakampis, supakuotas fcc, = veido pusė, centre - kubas (kubinis, tiesiogiai supakuotas). | |||||||
| *** Stabiliausias izotopas. | |||||||
| atominis skaičius | 2 | 10 | 18 | 36 | 54 | 86 | 118 |
| atominis svoris | 4.003 | 20.18 val | 39,948 | 83,8 | 131.293 | 222 | 294 *** |
| lydymosi temperatūra (° C) | −272,2 * | –248,59 | –189,3 | –157,36 | −111,7 | −71 | - |
| virimo temperatūra (° C) | −268,93 | –246,08 | –185,8 | –153,22 | –108 | −61,7 | - |
| tankis esant 0 ° C, 1 atmosfera (gramai litre) | 0,17747 | 0,899 | 1,784 | 3,75 | 5.881 | 9.73 | - |
| tirpumas vandenyje esant 20 ° C (kubiniai centimetrai dujų 1000 g vandens) | 8.61 | 10.5 | 33,6 | 59.4 | 108.1 | 230 | - |
| izotopų gausumas (sausumos, proc.) | 3 (0,000137), 4 (99,999863) | 20 (90,48), 21 (0,27), 22 (9,25) | 36 (0,3365), 40 (99,6003) | 78 (0,35), 80 (2,28), 82 (11,58), 83 (11,49), 84 (57), 86 (17,3) | 124 (0,09), 126 (0,09), 128 (1,92), 129 (26,44), 130 (4,08), 131 (21,18), 132 (26,89), 134 (10,44), 136 (8,87). | - | - |
| radioaktyvieji izotopai (masės skaičiai) | 5–10 | 16–19, 23–34 | 30–35, 37, 39, 41–53 | 69–77, 79, 81, 85, 87–100 | 110–125, 127, 133, 135–147 | 195–228 | 294 |
| dujinio išleidimo vamzdžio skleidžiamos šviesos spalva | geltona | raudona | raudona arba mėlyna | Geltona žalia | nuo mėlynos iki žalios | - | - |
| lydymosi šiluma (kilodžauliai vienam moliui) | 0,02 | 0,34 | 1.18 | 1,64 | 2.3 | 3 | - |
| garinimo šiluma (kalorijos vienam moliui) | 0,083 | 1,75 | 6.5 | 9.02 | 12.64 | 17 | - |
| savitoji šiluma (džauliai vienam gramui Kelvino) | 5.1931 | 1.03 | 0.52033 | 0,24805 | 0,15832 | 0,09365 | - |
| kritinė temperatūra (K) | 5.19 | 44.4 | 150,87 | 209,41 | 289,77 | 377 | - |
| kritinis slėgis (atmosfera) | 2.24 | 27,2 | 48.34 | 54.3 | 57,65 | 62 | - |
| kritinis tankis (gramai kubiniame centimetre) | 0,0696 | 0,4819 | 0,5356 | 0,9092 | 1.103 | - | - |
| šilumos laidumas (vatais į metrą Kelvinas) | 0,1513 | 0,0491 | 0.0177 | 0,0094 | 0,0057 | 0,0036 | - |
| magnetinis jautrumas (cg vienetai molyje) | –0.0000019 | –0.0000072 | –0.0000194 | –0.000028 | –0.000043 | - | - |
| kristalų struktūra ** | hcp | fcc | fcc | fcc | fcc | fcc | - |
| spindulys: atominis (angstromai) | 0,31 | 0,38 | 0,71 | 0,88 | 1.08 | 1.2 | - |
| spindulys: apskaičiuotas kovalentinis (kristalas) (angstromas) | 0,32 | 0,69 | 0,97 | 1.1 | 1.3 | 1.45 | - |
| statinis poliarizuotumas (kubiniai angstromai) | 0.204 | 0,392 | 1.63 | 2.465 | 4.01 | - | - |
| jonizacijos potencialas (pirmiausia, elektronų voltai) | 24.587 | 21.565 | 15.759 | 13.999 | 12.129 | 10.747 | - |
| elektronegatyvumas (Paulingas) | 4.5 | 4.0 | 2.9 | 2.6 | 2,25 | 2.0 | - |