Toris (Th), periodinės lentelės aktinoidų serijos radioaktyvusis cheminis elementas, atominis skaičius 90; tai yra naudingas branduolinio reaktoriaus kuras. Torį (1828 m.) Atrado švedų chemikas Jönsas Jacobas Berzelius. Jis yra sidabriškai baltas, bet, esant orui, tampa pilkas arba juodas. Jis yra maždaug perpus didesnis nei švinas ir yra tris kartus gausesnis nei uranas žemės plutoje. Toris komerciškai išgaunamas iš mineralinio monazito ir jame yra kitų mineralų, tokių kaip toritas ir torianitas. Torio metalas buvo pagamintas komerciniais kiekiais redukuojant tetrafluoridą (ThF 4) ir dioksidą (ThO 2) bei elektrolizuojant tetrachloridą (ThCl 4). Elementas buvo pavadintas norvegų dievu Thoru.

aktinoidinis elementas: praktinis aktinoidų pritaikymas
Toras taip pat gali turėti didelę ekonominę vertę, nes vieną iš jo izotopų, torį-232, galima paversti
Metalas gali būti išspaudžiamas, valcuotas, kaltas, keičiamas ir verpiamas, tačiau tempti sunku dėl mažo torio tempimo jėgos. Šioms ir kitoms fizinėms savybėms, tokioms kaip lydymosi ir virimo temperatūra, didelę įtaką daro nedideli tam tikrų priemaišų, tokių kaip anglies ir torio dioksidas, kiekiai. Toris pridedamas prie magnio ir magnio lydinių, kad būtų pagerintas jų stiprumas aukštoje temperatūroje. Jis buvo naudojamas komercinėse fotoelektrinėse elementuose matuojant ultravioletinę šviesą, kurios bangos ilgis svyruoja nuo 2000 iki 3750 angstromų. Įtrauktas į stiklą, toris suteikia aukšto lūžio rodiklio stiklus, naudingus specializuotoms optinėms reikmėms. Anksčiau jis buvo labai paklausus kaip dujinių ir žibalo lempų apvalkalų komponentas ir buvo naudojamas gaminant volframo siūlus lemputėms ir vakuuminiams vamzdžiams.
Torio radioaktyvumą (1898 m.) Savarankiškai nustatė vokiečių chemikas Gerhardas Carlas Schmidtas ir prancūzų fizikė Marie Curie. Natūralus toris yra radioaktyviųjų izotopų mišinys, daugiausia labai ilgaamžis toris-232 (pusinės eliminacijos laikas 1,40 × 10 10 metų), kuris yra torio radioaktyvaus skilimo serijos pradinė dalis. Kiti izotopai natūraliai randami urano ir aktino skilimo grupėse, o toris yra visose urano rūdose. Toris-232 yra naudingas selekciniuose reaktoriuose, nes fiksuodamas lėtai judančius neutronus jis skyla į dalijamąjį uraną-233. Parengti sintetiniai izotopai; toris-229 (7880 metų pusinės eliminacijos laikas), susiformavęs skilimo grandinėje, gaunamas iš sintetinio aktinoidinio elemento neptunio, yra paprastojo torio (torio-232) atsekamoji medžiaga.
Torio oksidacijos būsena yra +4 beveik visuose jo junginiuose. Th 4+ jonas sudaro daug sudėtingų jonų. Dioksidas (ThO 2), labai ugniai atspari medžiaga, gali būti naudojamas pramonėje; torio nitratą buvo galima įsigyti kaip komercinę druską.
Elemento savybės
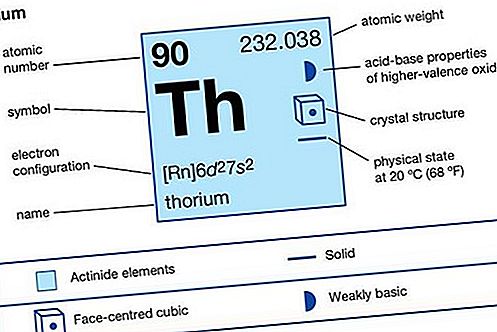
| atominis skaičius | 90 |
|---|---|
| atominis svoris | 232.038 |
| lydymosi temperatūra | apie 1700 ° C (3100 ° F) |
| virimo taškas | apie 4000 ° C (7200 ° F) |
| specifinė gravitacija | apie 11,66 (17 ° C) |
| oksidacijos būsena | +4 |
| dujinės atominės būsenos elektronų konfigūracija | [Rn] 6d 2 7s 2 |













