Efuzija
Apskaičiuodami dujų slėgį atsižvelkite į aukščiau aprašytą sistemą, tačiau A zoną rezervuaro sienoje pakeiskite maža skylute. Per skylę t bėgančių molekulių skaičius per t yra lygus (1/2) (N / V) v z (At). Šiuo atveju reikšmingi yra susidūrimai tarp molekulių, o rezultatas galioja tik mažoms skylėms labai plonose sienose (palyginti su vidutiniu laisvu keliu), kad šalia skylės priartėjusi molekulė patektų pro šalį nesikišdama į kitą molekulę ir būdamas atitrauktas. Ryšys tarp v z ir vidutinio greičio v̄ yra gana aiškus: v z = (1/2) v̄.
Palyginus dviejų skirtingų dujų, išsiskiriančių iš tos pačios skylės, greitį, pradedant nuo to paties dujų tankio kiekvieną kartą, nustatoma, kad daug daugiau lengvųjų dujų nei sunkiųjų dujų, ir daugiau dujų išeina aukštoje temperatūroje nei žemoje temperatūroje., kiti dalykai yra lygūs. Visų pirma,
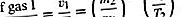
Paskutinis žingsnis išplaukia iš energijos formulės: (1/2) mv 2 = (3/2) kT, kur (v 2) 1/2 yra artimas v, nors v 2 ir (v̄) 2 iš tikrųjų skiriasi skaitinis faktorius, artimas vienybei (būtent, 3π / 8). Šį rezultatą 1846 m. Eksperimentiškai atrado Grahamas, esant pastoviai temperatūrai, ir jis yra žinomas kaip Grahamo efuzijos dėsnis. Jis gali būti naudojamas matuojant molekulinius svorius, matuojant medžiagos, kurios žemas garų slėgis, garų slėgį arba apskaičiuojant molekulių išgarinimo greitį iš skysto ar kieto paviršiaus.
Šiluminis transpiracija
Tarkime, kad du tų pačių dujų, bet skirtingos temperatūros konteineriai yra sujungti maža skylute ir kad dujos yra pastovios. Jei skylė yra pakankamai maža, o dujų tankis yra pakankamai mažas, kad įvyktų tik efuzija, pusiausvyros slėgis būtų didesnis aukštoje temperatūroje. Jei pradinis slėgis abiejose pusėse yra vienodas, dujos tekės iš žemos temperatūros pusės į aukštą, todėl padidės aukšto slėgio slėgis. Pastaroji situacija vadinama terminiu transpiracija, o pastovios būsenos rezultatas vadinamas termomolekulinio slėgio skirtumu. Šie rezultatai išplaukia iš efuzijos formulės, jei naudojamas idealus dujų dėsnis, pakeičiant N / V p / T;
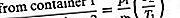
Pasiekus pastovią būseną, efuzijos greitis yra lygus, taigi
Šį reiškinį pirmą kartą eksperimentiškai ištyrė Osbornas Reynoldsas 1879 m. Mančesteryje. Klaidų gali kilti, jei dujų slėgis indelyje matuojamas esant labai žemai ar labai aukštai temperatūrai, per smulkų vamzdelį prijungus jį prie manometro kambario temperatūroje. Nepertraukiamą dujų cirkuliaciją galima sukurti sujungus du konteinerius su kitu vamzdžiu, kurio skersmuo yra didelis, palyginti su vidutiniu laisvu keliu. Dėl slėgio skirtumo dujos per šį vamzdelį teka klampiu srautu. Šilumos variklis, pagrįstas tokiu cirkuliuojančiu srautu, deja, yra mažai efektyvus.








![Jaffos mūšis Europos istorija [1192] Jaffos mūšis Europos istorija [1192]](https://images.thetopknowledge.com/img/world-history/4/battle-jaffa-european-history-1192.jpg)


