Selenas (se), cheminis elementas, esantis deguonies grupėje (periodinės lentelės 16 grupė [VIa]), savo cheminėmis ir fizinėmis savybėmis glaudžiai susijęs su sieros ir telūro elementais. Selenas yra retas, sudaro maždaug 90 dalių milijardui Žemės plutos. Retkarčiais jis randamas nesujungtas, pridedamas prie vietinės sieros, tačiau dažniausiai randamas kartu su sunkiaisiais metalais (variu, gyvsidabriu, švinu ar sidabru) keliuose mineraluose. Pagrindinis komercinis seleno šaltinis yra šalutinis vario rafinavimo produktas; Pagrindiniai jo naudojimo būdai yra elektroninės įrangos, pigmentų ir stiklo gamyba. Selenas yra metaloidas (elementų tarpinis elementas tarp metalų ir nemetalų). Pilka metalinė elemento forma yra stabiliausia įprastomis sąlygomis; ši forma turi neįprastą savybę - labai padidėja elektros laidumas veikiant šviesai. Seleno junginiai yra toksiški gyvūnams; augalai, auginami seleniferiniame dirvožemyje, gali sukoncentruoti elementą ir tapti nuodingi.
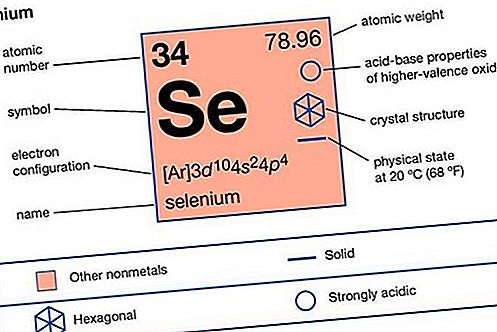

deguonies grupės elementas: natūralus atsiradimas ir jo panaudojimas
Elementas selenas (simbolis Se) yra daug retesnis nei deguonis ar siera, sudarytas iš apytiksliai 90 dalių milijardui plutos.
.Elemento savybės
| atominis skaičius | 34 |
|---|---|
| atominis svoris | 78,96 |
| stabilių izotopų masės | 74, 76, 77, 78, 80, 82 |
| lydymosi temperatūra | |
| amorfinis | 50 ° C (122 ° F) |
| pilka | 217 ° C (423 ° F) |
| virimo taškas | 685 ° C (1 265 ° F) |
| tankis | |
| amorfinis | 4,28 gramo / cm 3 |
| pilka | 4,79 gramo / cm 3 |
| oksidacijos būsenos | −2, +4, +6 |
| elektronų konfigūracija | 1s 2 2s 2 2p 6 3s 2 3p 6 3d 10 4s 2 4p 4 |
Istorija
1817 m. Švedų chemikas Jöns Jacob Berzelius pastebėjo raudoną medžiagą, susidarančią dėl sulfido rūdų, gautų iš Švedijos Faluno kasyklų. Kai ši raudona medžiaga buvo ištirta kitais metais, ji pasirodė esanti elementas ir buvo pavadinta Mėnulio ar Mėnulio deivės Selene vardu. Rūdą, kuriame neįprastai didelis seleno kiekis, Berzelius atrado tik kelias dienas prieš tai, kai jis pasaulio mokslinėms visuomenėms pateikė pranešimą apie seleną. Jo humoro jausmas išryškėja pavadinime, kurį jis davė rūdai, eukairitui, reiškiančiam „tik laiku“.
Atsiradimas ir panaudojimas
Seleno dalis žemės plutoje sudaro nuo 10–5 iki 10–6 procentų. Jis daugiausia gaunamas iš anodo nuosėdų (nuosėdų ir anodo liekanų) iš vario ir nikelio elektrolitinio rafinavimo. Kiti šaltiniai yra vario ir švino gamybos dūmtakio dulkės ir dujos, susidariusios kepant piritus. Selenas pridedamas prie vario rafinuojant tą metalą: apie 40 procentų pradinio rūdos seleno gali susikaupti varyje, nusodintame elektrolitinių procesų metu. Iš tonos išlydyto vario galima gauti apie 1,5 kilogramo seleno.
Kai selenas nedideliais kiekiais įpilamas į stiklą, jis naudojamas kaip spalviklis; didesniais kiekiais jis stiklui suteikia aiškią raudoną spalvą, naudingą signalinėse lemputėse. Šis elementas taip pat naudojamas gaminant keramikos ir plieno dirbinius iš raudonų emalių, taip pat gumos vulkanizavimui, siekiant padidinti atsparumą dilimui.
Seleno rafinavimo pastangos yra didžiausios Vokietijoje, Japonijoje, Belgijoje ir Rusijoje.
Allotropija
Seleno allotropija nėra tokia plati kaip sieros, o allotropai nebuvo ištirti taip nuodugniai. Tik dvi kristalines seleno atmainas sudaro ciklinės Se 8 molekulės: žymimos α ir β, abi egzistuoja kaip raudoni monoklininiai kristalai. Pilka allotrope, turinti metalinių savybių, susidaro išlaikant bet kurią kitą formą 200–220 ° C temperatūroje ir yra stabiliausia įprastomis sąlygomis.
Amorfos (nekristalinės), raudonos spalvos miltelių pavidalo selenas gaunamas, kai seleno rūgšties arba vienos iš jos druskų tirpalas yra apdorojamas sieros dioksidu. Jei tirpalai yra labai praskiesti, šios rūšies ypač smulkios dalelės suteikia skaidrią raudoną koloidinę suspensiją. Skaidrus raudonas stiklas gaunamas panašiu būdu, kuris vyksta, kai išlydytas stiklas, kuriame yra selenitų, yra apdorojamas anglimi. Stiklinė, beveik juoda seleno rūšis susidaro greitai aušinant kitas modifikacijas, kai temperatūra viršija 200 ° C. Ši stiklakūnio forma virsta raudonais, kristaliniais alotropais, kaitinant ją aukštesnėje nei 90 ° C temperatūroje arba palaikant sąlytį su organiniais tirpikliais, tokiais kaip chloroformas, etanolis ar benzenas.
Paruošimas
Grynas selenas gaunamas iš nuosėdų ir dumblo, susidarančio gaminant sieros rūgštį. Nešvarus raudonasis selenas ištirpinamas sieros rūgštyje, dalyvaujant oksidatoriui, tokiam kaip kalio nitratas ar tam tikri mangano junginiai. Tiek selenu, H 2 SeO 3, ir selenic rūgšties, H 2 SeO 4, yra suformuotas ir gali būti išplaunamas iš liekamojo netirpių medžiagų. Kiti metodai apima oksidaciją oru (skrudinimą) ir kaitinimą natrio karbonatu, kad būtų gautas tirpus natrio selenitas, Na 2 SeO 3 · 5H 2 O ir natrio selenatas, Na 2 SeO 4. Chloro taip pat gali būti naudojamas: jos poveikis po metalo selenidų gamina lakiųjų junginių, įskaitant seleno dichlorido, SeCl 2; seleno tetrachlorido, SeCl 4; diselenium dichloridas, Se 2 Cl 2; ir selenas oksichloridas, SeOCl 2. Viename procese šie seleno junginiai vandenyje virsta silpna rūgštimi. Selenas galutinai išgaunamas, apdorojant silpną rūgštį sieros dioksidu.
Selenas yra dažnas rūdų komponentas, vertinamas pagal sidabro ar vario kiekį; jis sukoncentruojamas nuosėdose, nusėdusiose metalų elektrolitinio gryninimo metu. Buvo sukurti metodai atskirti seleną nuo šių gleivių, kuriuose taip pat yra šiek tiek sidabro ir vario. Lydydamasis gleives, susidaro sidabro selenidas, Ag 2 Se ir vario (I) selenidas, Cu 2 Se. Šiuos selenidus apdorojant hipo chloro rūgštimi HOCl, gaunami tirpūs selenitai ir selenatai, kuriuos galima redukuoti sieros dioksidu. Galutinis seleno valymas atliekamas pakartotinai distiliuojant.
Fizikinės ir elektrinės savybės
Ryškiausia kristalinio seleno fizinė savybė yra jo fotolaidumas: apšviečiant elektrinis laidumas padidėja daugiau nei 1000 kartų. Šis reiškinys atsiranda dėl santykinai silpnai laikomų elektronų skatinimo ar sužadinimo šviesoje iki aukštesnės energijos būsenų (vadinamų laidumo lygiais), leidžiančiomis elektronų migraciją, taigi ir elektrinį laidumą. Priešingai, tipiškų metalų elektronai jau yra laidumo lygiuose ar juostose, galintys tekėti veikiant elektromotorinei jėgai.
Elektrinis seleno varža kinta labai dideliu diapazonu, atsižvelgiant į tokius kintamuosius kaip alotropo pobūdis, priemaišos, rafinavimo būdas, temperatūra ir slėgis. Dauguma metalų netirpsta selene, o nemetalinės priemaišos padidina varžą.
Kristalinio seleno apšvietimas 0,001 sekundės padidina jo laidumą 10–15 kartų. Raudona šviesa yra efektyvesnė už trumpesnio bangos ilgio šviesą.
Šios seleno fotoelektrinės ir fotojautrumo savybės yra pranašesnės, statant įvairius prietaisus, kurie šviesos stiprio pokyčius gali paversti elektros srove, o vėliau - vizualiais, magnetiniais ar mechaniniais. Signalizacijos įtaisai, mechaniniai atidarymo ir uždarymo įtaisai, saugos sistemos, televizija, garso filmai ir kserografija priklauso nuo seleno puslaidininkio savybių ir fotojautrumo. Kintamosios elektros srovės ištaisymas (pavertimas į nuolatinę srovę) daugelį metų buvo vykdomas seleno valdomomis priemonėmis. Daugelį fotoelementų, naudojančių seleną, pakeitė kiti prietaisai, kuriuose naudojamos jautresnės, lengviau prieinamos ir lengviau pagaminamos medžiagos nei selenas.