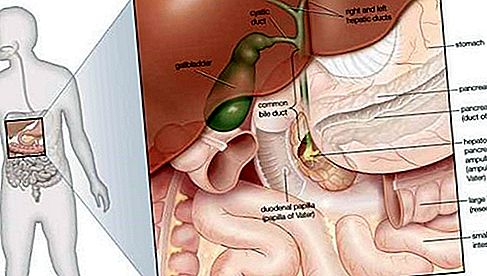
Fluoras (F), labiausiai reaktyvusis cheminis elementas ir lengviausias halogeninių elementų narys, arba 17 periodinės lentelės grupė (VIIa grupė). Jos cheminį aktyvumą galima priskirti dėl jo ypatingo sugebėjimo pritraukti elektronus (jis yra labiausiai elektroneigiamas elementas).) ir mažais jo atomų dydžiais.
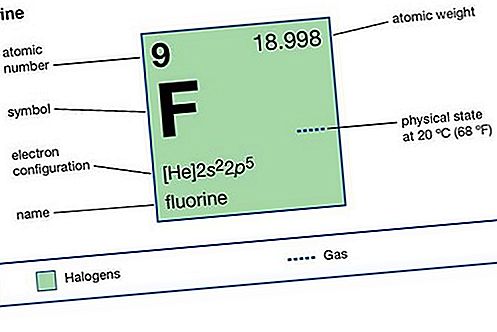
Elemento savybės
| atominis skaičius | 9 |
|---|---|
| atominis svoris | 18.9984 |
| lydymosi temperatūra | –219,62 ° C (–363,32 ° F) |
| virimo taškas | –188 ° C (–306 ° F) |
| tankis (1 atm, 0 ° C arba 32 ° F) | 1,696 g / litre (0,226 uncijos / galonui) |
| oksidacijos būsenos | −1 |
| elektronų konfigūracija. | 1s 2 2s 2 2p 5 |
Istorija
Mineralinis fluoras (arba fluoras), kurio sudėtyje yra fluoro, 1529 m. Buvo aprašytas vokiečių gydytojo ir mineralogisto Georgius Agricola. Panašu, kad neapdorotą vandenilio fluorido rūgštį pirmą kartą paruošė nežinomas anglų stiklo gamintojas 1720 m. 1771 m. Švedų chemikas Carlas Wilhelmas Scheele nevalytą vandenilio fluoridą pagamino kaitindamas fluoro mišinį koncentruota sieros rūgštimi stikliniame retortyje, kurį labai sugadino produktas; dėl to indai, pagaminti iš metalo, buvo naudojami vėlesniuose eksperimentuose su medžiaga. Beveik bevandenė rūgštis buvo paruošta 1809 m., O po dvejų metų prancūzų fizikas André-Marie Ampère pasiūlė, kad tai vandenilio junginys su nežinomu elementu, analogišku chlorui, kuriam jis pasiūlė pavadinimą fluoras. Tada fluoropadas buvo pripažintas kalcio fluoridu.
Fluoro išskyrimas ilgą laiką buvo viena pagrindinių neišspręstų neorganinės chemijos problemų, ir tik 1886 m. Prancūzų chemikas Henri Moissan paruošė elementą elektrolizuodamas kalio vandenilio fluorido tirpalą vandenilio fluoride. Už fluoro išskyrimą jis gavo 1906 m. Nobelio chemijos premiją. Sunkumas tvarkant elementą ir jo toksinės savybės prisidėjo prie lėto fluoro chemijos progreso. Tiesą sakant, iki Antrojo pasaulinio karo elementas buvo laboratorinis smalsumas. Tačiau tada, kai urano heksafluoridas buvo naudojamas atskirti urano izotopus, kartu su pramoninės svarbos organinių fluoro junginių kūrimu, fluoras tapo nemaža naudojimo pramonės chemine medžiaga.
Atsiradimas ir pasiskirstymas
Fluoro turintis mineralinis fluoras (fluoras, CaF 2) šimtmečius buvo naudojamas kaip srautas (valymo priemonė) įvairiuose metalurgijos procesuose. Pavadinimas fluorspar yra kilęs iš lotyniško fluere, „tekėti“. Vėliau mineralas pasirodė esąs elemento, atitinkamai pavadinto fluoru, šaltinis. Bespalviai, skaidrūs fluoro pluošto kristalai apšviečiami melsvu atspalviu, todėl ši savybė vadinama fluorescencija.
Fluoras gamtoje randamas tik kaip jo cheminiai junginiai. Išskyrus kai kuriuos laisvojo elemento kiekius fluorescenciniame šparage, kurį veikė radis. Tai nėra retas elementas, jis sudaro apie 0,065 proc. Žemės plutos. Pagrindiniai mineralai, kurių sudėtyje yra fluoro, yra (1) fluoras, kurio indėliai susidaro Ilinojaus valstijoje, Kentukyje, Derbišyre, Vokietijos pietuose, Prancūzijos pietuose ir Rusijoje, ir pagrindinis fluoro šaltinis, (2) kriolitas (Na 3 AlF 6). daugiausia iš Grenlandijos, (3) fluoroapatitas (Ca 5 [PO 4] 3 [F, Cl]), plačiai paplitęs ir turintis įvairius fluoro ir chloro kiekius, (4) topazas (Al 2 SiO 4 [F, OH] 2)), brangakmenio ir (5) lepidolito, žėručio, taip pat gyvūnų kaulų ir dantų komponento.